首页 > 财经新闻/ 正文
在约10%的癌症中丝氨酸/苏氨酸激酶AKT发生了突变,这很大程度的说明了其在癌症中的致癌作用。除了AKT基因突变外,生长因子上游信号通路的失调常常能够激活癌细胞中的AKT。
GSK3β、FOXO和TSC2是AKT的三个主要的下游基因,其能够介导AKT对不同刺激的响应并行使多种功能。既往研究显示,AKT介导的TSC2磷酸化和抑制作用已被认为是AKT激活mTORC1(雷帕霉素复合物1)的主要机制。
mTORC1是细胞响应生长因子和营养素进行细胞增殖的中心调控因子,其在癌症中表达失调。精氨酸能够激活mTORC1。
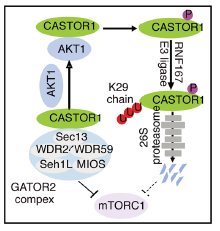
相关机制示意图
CASTOR1(mTORC1亚基1)是一种新发现的胞质精氨酸传感器,其可对精氨酸响应并调节mTORC1的活性。有趣的是,高水平的CASTOR1蛋白会抑制AAS(包括精氨酸)对mTORC1的激活。由于癌细胞常处于低营养水平状态,因此可能存在另一种机制来调控CASTOR1的表达。
在该研究中,研究人员发现E29泛素连接酶RNF167能够对CASTOR1进行K29连接的多泛素化和降解。此外,AKT能够介导CASTOR1 S14位点的磷酸化,显著增加其与RNF167的结合,促进其泛素化和降解,并降低其对MIOS的亲和力,从而导致mTORC1的激活。因此说明AKT可通过TSC2和CASTOR1依赖性途径来激活mTORC1。
RNF167介导的泛素化和AKT1介导的磷酸化促进乳腺癌的发生发展
进一步的研究显示,几种具有较高CASTOR1表达的细胞类型对精氨酸的调节并不敏感。值得注意的是,AKT和RNF167介导的CASTOR1降解能够激活独立于精氨酸的mTORC1,并最终促进乳腺癌的发生发展。
总而言之,该研究结果揭示了mTORC1的相关调节机制,并将RNF167鉴定为mTORC1失调相关疾病的治疗靶标。
原始出处:
Li, T., Wang, X., Ju, E. et al. RNF167 activates mTORC1 and promotes tumorigenesis by targeting CASTOR1 for ubiquitination and degradation. Nat Commun 12, 1055 (16 February 2021).
- 搜索
-
- 1000℃游族网络:董事长林奇逝世 公司将尽快推举董事长人选
- 1000℃20年来首次!民生银行高管集体增持 重磅信号浮现?招商、中信高管也岀手 机构火线解读
- 1000℃?第二季! 被解散的董事会秘书公开反击,请愿书要求取消董事会决议国信金融控股回应:将积极回应
- 1000℃?“环球银行”行长顾Shu接任周母兵,并将成为四大银行中最年轻的董事长。 高级会计专家如何指导中国农业银行?
- 1000℃?阿里巴巴股票持续下跌
- 1000℃?400亿铅电池领导者天能股份在科技创新局,“永进”,硅谷天堂等明星股东上市
- 1000℃?德意志银行成为北京首家获准托管证券投资基金的外资银行
- 1000℃?顾Shu担任农业银行党委书记,将成为四大银行中最年轻的董事长
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)